ثنائي أمين الإيثيلين رباعي حمض الخل
| ثنائي أمين الإيثيلين رباعي حمض الخل | |
|---|---|

| |
| |
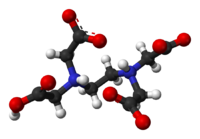
2,2',2'',2'''-(ethane-1,2-diyldinitrilo)tetraacetic acid | |
Other names EDTA, H4EDTA, ثنائي أمين الإيثلين - رباعي حمض الخل. | |
| المعرفات | |
| رقم CAS | |
| بوبكيم (PubChem) | |
| ChemSpider | 5826 |
| RTECS number | AH4025000 |
| Jmol-3D images | Image 1 |
| |
| |
| الخصائص | |
| الصيغة الجزيئية | C10H16N2O8 |
| كتلة مولية | 292.2 g mol-1 |
| الكثافة | 0.86 غ/سم3 |
| نقطة الانصهار |
237–245 °م (dec.) |
| الحموضة (pKa) | pK1=0.0 (CO2H) (µ=1.0) pK2=1.5 (CO2H) (µ=0.1) pK3=2.00 (CO2H) (µ=0.1) pK4=2.69 (CO2H) (µ=0.1) pK5=6.13 (NH+) (µ=0.1) pK6=10.37 (NH+) (µ=0.1)[1] |
| المخاطر | |
| MSDS | صحيفة خارجية (en) |
| R-phrases | R36 |
| S-phrases | S26 |
| Main hazards | مهيج |
| NFPA 704 | |
| في حال عدم ذكر الشروط فإن
البيانات الواردة أعلاه مقاسة في الشروط النظامية ومدونة حسب النظام الدولي للوحدات | |
ثنائي أمين الإيثيلين رباعي حمض الخل والذي يرمز له اختصاراً EDTA وهو مركب كيميائي من فئة الأحماض الكربوكسيلية عديدة الأمين (polyamino carboxylic acid)، ويسمى الأساس المترافق بـ رباعي خلات ثنائي أمين الإيثلين (ethylenediaminetetraacetate). "إي دي تي إيه " هو صلب ذواب في الماء ولا لون له. ويستخدم بكثرة في إزالة الترسبات الملحية (Limescale) على جدارن الغلايات. وتأتي أهميته بسبب دوره كمتمخلب، أي أنه قادر على احتجاز الأيونات المعدنية مثل Ca2+ و Fe3+. وتبقى الأيونات المعدنية في المحلول بعد ارتباطها بـ إي دي تي آ ولكنها تبدي تفاعلية أقل. ينتج إي دي تي آ كأملاح متعددة، وخصوصا إي دي تي آ ثنائي الصوديوم، وإي دي تي آ ثنائي الصوديوم كالسيوم.
الاستخدامات
استخدامات صناعية
يستخدم إي دي تي آ كعامل احتجاز (sequestering agent) للشوارد المعدنية في المحاليل المائية. وفي صناعة النسيج يستخدم إي دي تي آ لمنع الشوراد المعدنية من تغيير لون المواد المصبوغة. وفي صناعة الورق، يمنع إي دي تي آ قابلية الشوارد المعدنية وخصوصا Mn2+ من تحفيز عدم تناسب (disproportionation) فوق أكسيد الهيدروجين، التي تستخدم في التبييض بدون الكلور. وبطريقة مشابهة، يضاف إي دي تي آ إلى بعض الطعام كمادة حافظة لمنع تحفيز عملية تغير اللون الناتجة عن الأكسدة، التي تحفز نتيجة الشوارد المعدنية[2].
وفي مواد العناية الشخصية، يضاف إي دي تي آ إلى مواد التجميل لتحسين استقرارها عند تماسها مع الهواء[3]. والمشروبات الغازية الحاوية على حمض الأسكوربيك وبنزوات الصوديوم، فإن إي دي تي آ تخفف من تشكيل البنزين وهي مادة مسرطنة[4].
المراجع
- ↑ Harris, D.C. "Quantitative Chemical Analysis", 7th ed., W. H. Freeman and Compagny, New York, 2007
- ↑ Furia T (1964). "EDTA in Foods — A technical review". Food Technology. 18 (12): 1874–1882.
- ↑ Lanigan RS and Yamarik TA (2002). "Final report on the safety assessment of EDTA, calcium disodium EDTA, diammonium EDTA, dipotassium EDTA, disodium EDTA, TEA-EDTA, tetrasodium EDTA, tripotassium EDTA, trisodium EDTA, HEDTA, and trisodium HEDTA". Int J Toxicol. 21 Suppl 2: 95–142. PMID 12396676. doi:10.1080/10915810290096522.
- ↑ US Food and Drug Administration: Center for Food Safety and Applied Nutrition أسئلة وأجوبة عن وجود البنزين في المشروبات الغازية والمشروبات الأخرى
وصلات خارجية
- Lanigan RS, Yamarik TA (2002). "Final report on the safety assessment of EDTA, calcium disodium EDTA, diammonium EDTA, dipotassium EDTA, disodium EDTA, TEA-EDTA, tetrasodium EDTA, tripotassium EDTA, trisodium EDTA, HEDTA, and trisodium HEDTA". Int. J. Toxicol. 21 Suppl 2: 95–142. PMID 12396676. doi:10.1080/10915810290096522.
- pH-Spectrum of EDTA complexes
- EDTA: Molecule of the Month
- EDTA Determination of Total Water Hardness
- 507 references regarding oral EDTA
- EDTA: the chelating agent under environmental scrutiny, Química Nova, Nov.-Dec., 2003 (text version)
- EDTA: the chelating agent under environmental scrutiny, Química Nova, Nov.-Dec., 2003 (PDF version)
| المزيد من الصور والملفات في كومنز عن: ثنائي أمين الإيثيلين رباعي حمض الخل |
