حرائك دوائية
الحرائك الدوائية أو الحركيات الدوائية (بالإنجليزية: Pharmacokinetics) هي دراسة حركة الدواء ضمن العضوية أي انتقاله والتغيرات التي تطرأ عليه مع الزمن منذ دخوله العضوية إلى لحظة إطراحه منها. يختصر بالحرفين “PK” ليشكل أحد فروع علم الأدوية والصيدلة المتجهة لتحديد مصير المواد الدوائية التي تقدم للمتعضية الحية.
بشكل عملي، يهتم هذا العلم بالمركبات الدوائية عامة والتغيرات التي تحصل عليها ضمن العضوية رغم أن طرائق البحث فيه يمكن تطبيقها على أية مادة كيميائية، يتم هضمها أو يتم تقديمها وإدخالها للعضوية.
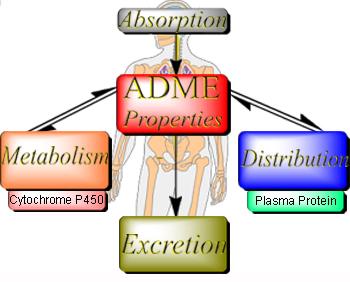
يؤثر الجسم على المادة الدوائية في أربعة مراحل رئيسية، هي: الامتصاص والتوزع والاستقلاب والإطراح.
الامتصاص
هو انتقال الدواء و وصوله إلى الدوران العام، و يكون تاماً و سريعاً في حال الحقن الوريدي، أما في حالات أخرى كالإعطاء الفموي فيختلف الامتصاص حسب عوامل أخرى ( انحلاليته – مروره عبر الأغشية الخلوية للخلايا المعوية – وصوله إلى الدوران العام.....الخ) ويمكن ان تتم عملية الامتصاص بطريقتين:
- الانتشار المنفعل، ويمتاز بأنه:
- يكون من التركيز المرتفع إلى التركيز المنخفض.
- غير قابل للاشباع.
- لا يحتاج إلى طاقة.
- النقل الفعال، ويمتاز بأنه:
- يكون عن طريق الأنظيمات و البروتينات الناقلة، الموجودة على الأاغشية الخلوية، والتي تحمل المواد الدوائية و تدخلها إلى الحيز الآخر من الغشاء.
- تحتاج إلى طاقة.
التوزع
هو انتقال الدواء من الدوران العام إلى النسج والخلايا المستهدفة.
الاستقلاب
هو آلية هامة يتمكن من خلالها الجسم من إنهاء تأثير أو التخفيف أو زيادة فعالية المركب الدوائي. أو قد يجعل من المركب الدوائي أكثر قابلية للانطراح من الجسم، ويعتبر الكبد هو المركز الرئيسي لعملية الاستقلاب في الجسم.
طورت الحيوانات جمل معقدة تقوم بإزالة سمية المواد الكيميائية الغريبة ("الأجنبية بيولوجياً xenobiotics")، متضمنة المسرطنات والذيفانات الموجودة في النباتات السامة. تعد الأدوية حالة خاصة من هذه المواد الأجنبية بيولوجياً xenobiotics ومثل القلويدات النباتية غالباً ما تظهر عدم تناظر مرآتي chirality(أي أن هناك أكثر من مصاوغ فراغي)، مما يؤثر على استقلابها الكلي. يضم الاستقلاب الدوائي نوعين من التفاعلات يعرفون بالطور الأول والطور الثاني. يحصل هذين الطورين بالتعاقب غالباً، إلا أن هذا ليس شيئاً ثابتاً. ينقص كلا الطورين الانحلالية بالدسم وبالتالي يزيدان من الإطراح الكلوي.
تفاعلات الطور الأول
تفاعلات الطور الأول تقويضية (مثلاً الأكسدة أو الإرجاع أو الحلمهة) وتكون المنتجات غالباً أكثر تفاعلية كيميائياً وبالتالي أكثر سمية أو سرطنة أحياناً من الدواء الأصل. تدخل تفاعلات الطور الأول غالباً جزيئة تفاعلية مثل هيدروكسيل إلى الجزيئية في عملية تعرف بـ "وضع وظيفة functionalisation". تساعد هذه المجموعة بعد ذلك كنقطة هجوم لجملة الاقتران لترفق متبادل مثل غلُوكُورونيد، مما يشرح لماذا غالباً ما تسبق تفاعلات الطور الأول تفاعلات الطور الثاني. تحصل تفاعلات الطور الأول بشكل أساسي في الكبد. تكون العديد من الأنزيمات الكبدية المستقلبة للأدوية، بما فيها أنزيمات CYP، مغروسة في الشبكة الهيولية الباطنية الملساء. تدعى هذه الأنزيمات غالباً الأنزيمات "الصغروية" لأن الشبكة الهيولية الباطنية تتكسر على المجانسة والتثفيل التفريقي إلى شدف صغيرة تترسب فقط بعد تثفيل مطول عالي السرعة في الجزء الصغروي. يجب على الدواء عبور الغشاء البلازمي ليصل إلى هذه الأنزيمات المستقلبة في الأحياء. تقوم الجزيئات القطبية بذلك بشكل أقل سهولة من الجزيئات غير القطبية باستثناء إن كان هناك آليات ناقلة نوعية، وبالتالي فإن الاستقلاب داخل الخلوي مهم للأدوية المنحلة في الدسم، في حين أن الأدوية القطبية تطرح غير متغيرة في البول على الأقل جزئياً.
جملة أحادي الأكسجيناز P450
طبيعة أنزيمات P450 وتصنيفها وآليتها.
الجدول 9-1. أمثلة لأدوية تعد ركائز لإيزوأنزيمات P450¬.
| Isoenzyme P450 | Drug(s) |
|---|---|
| CYP1A2 | Caffeine, paracetamol (→NAPQI), tacrine, theophylline |
| CYP2B6 | Cyclophosphamide, methadone |
| CYP2C8 | Paclitaxel, repaglinide |
| CYP2C19 | Omeprazole, phenytoin |
| CYP2C9 | Ibuprofen, tolbutamide, warfarin |
| CYP2D6 | Codeine, debrisoquine, S-metoprolol |
| CYP2E1 | Alcohol, paracetamol |
| CYP3A4, 5, 7 | Ciclosporin, nifedipine, indinavir, simvastatin |
أنزيمات السيتوكروم P450 هي بروتينات هيم، وتؤلف عائلة كبيرة (superfamily) من الأنزيمات ذات القرابة لكنها أنزيمات متميزة، يشار إلى كل منها بـ CYP متبوعاً بمجموعة محددة من الأعداد وحرف. تختلف هذه الأنزيمات عن بعضها بتسلسل الحموض الأمينية، وبالحساسية للعوامل المثبطة والمحرضة، وبنوعية التفاعلات التي تحفزها. الأفراد المختلفة من العائلة ذات نوعيات ركائز مختلفة لكنها متراكبة، وقد يعمل على نفس الركيزة لكن بمعدلات مختلفة. تشكل تنقية أنزيمات P450 وتنسيل الدنا المتمم أسس التصنيف الحالي، الذي يرتكز على تشابهات التسلسل الحمضي الأميني. وصفت 74 عائلة من جينة CYP، وثلاثة عائلات أساسية منها متضمنة في الاستقلاب الدوائي في الكبد البشري (CYP1, CYP2, CYP3). أمثلة عن الأدوية العلاجية التي تعد ركازات لبعض إيزوأنزيمات P450 الهامة موجودة في الجدول 9.1. تتطلب أكسدة الدواء بواسطة جملة أحادي الأكسجيناز P450: دواء (ركازة، DH)، و P450 وأكسجين جزيئي وNADPH وفلافوبروتين (NADH-P450 reductase). تضم الآلية حلقة معقدة، لكن التأثير الكلي الناتج عن التفاعل بسيط جداً وهو: إضافة ذرة أكسجين (من الأكسجين الجزيئي) إلى الدواء لتشكيل مجموعة هدروكسيل (منتج DOH)، والذرة الأخرى من الأكسجين تتحول إلى ماء. أنزيمات P450 ذات خصائص طيفية مميزة، وتندمج الأشكال المرجعة مع أحادي أكسيد الكربون لتشكيل مركب زهري (ومن هنا أتت P من pink) مع امتصاص قريب من 450 nm (مجال 447-452 nm). الدليل الأول على أن هناك أكثر من شكل من CYP أتى من ملاحظة أن معالجة الجرذان بـ 3-methylcholanthrene (3-MC)، عامل محرض، يؤدي إلى انزياح في الامتصاص الأعظمي من 450 إلى 448 nm، إذ يمتص الشكل الإسوي isoform المحرض بـ 3-MC من الأنزيم الضوء بشكل أعظمي عند طول موجة أقصر بقليل من الأنزيم غير المحرض.
P450 والاختلاف البيولوجي
- هناك اختلافات مهمة في التعبير عن أنزيمات P450 وتنظيمها بين الأنواع. مثلاً، المسالك التي تولد بها أمينات غذائية متغايرة الحلقة معينة (تتشكل عندما يطبخ اللحم) مركبات سامة جينياً تتضمن فرداً من العائلة الكبيرة P450 وهو (CYP1A2) وهو يتواجد بشكل أساسي لدى البشر والجرذان (التي تطور أورام قولونية بعد المعالجة بهذه الأمينات) لكنه لا يتواجد في قرود الرباح (التي لا تطور أورام قولونية بعد المعالجة بهذه الأمينات).
- لهذه الاختلافات بين الأنواع مقتضيات هامة لاختيار النوع المستعمل لاختبار السمية والتسرطن خلال تطوير أدوية للاستعمال في البشر. هناك مصادر كبيرة للاختلافات بين الأفراد في أنزيمات P450 ضمن المجتمعات البشرية مما له أهمية كبيرة في المداواة.
- تضم هذه الاختلافات تعددات أشكال جينية (تسلسلات بديلة في موضع ضمن أليلات طاق الـ DNA والتي تظل مستمرة في مجتمع عبر عدة أجيال). العوامل البيئية مهمة أيضاً، بما أن المثبطات الأنزيمية والمحرضات متواجدة في القوت والبيئة. مثلاً، يثبط مكون في عصير الجريب فروت الاستقلاب الدوائي (مما يؤدي إلى نتائج كارثية محتملة، بما فيها اضطرابات نظمية قلبية)، في حين أن براعم بروكسل ودخان السجائر تحرض أنزيمات P450.
- تحرض مكونات عشبة القديس جون (مستعملة لعلاج الاكتئاب في الطب البديل) إيزونزيمات CYP450 بالإضافة P-glycoprotein (P-gp).
- لا تضم جميع تفاعلات الأكسدة الدوائية جملة الـ P450: تستقلب بعض الأدوية في البلازما (مثلاً حلمهة suxamethonium بواسطة الكولين إستراز البلازمي) أو الرئة (مثلاً مختلف الـ prostanoids) أو الأمعاء (مثلاً التيرامين, ال[[سالبوتامول]).
- يستقلب الإيثانول بواسطة أنزيم هيولي منحل، نازعة هدروجين الكحول، بالإضافة إلى CYP2E1. *الأنزيمات الأخرى المعتمدة على P450¬ المتضمنة في أكسدة الدواء تشمل الكزانتين أكسيداز، الذي يعطل 6-مركابتوبورين، والأكسيداز أحادي الأمين، الذي يعطل العديد من الأمينات الفعالة بيولوجياً (مثل النورأدريالين نورإيبنفرين، التيرامين، 5-هدروكسيتربتامين).
- لا تضم التفاعلات المحلمهة (مثل الأسبرين) أنزيمات كبدية صغروية لكن تحصل في البلازما وفي عدة أنسجة. كل من الروابط الإسترية و(بشكل أقل سهولة) الأميدية عرضة للحلمهة.
- التفاعلات الإرجاعية أقل شيوعاً بكثير من الأكسدة، لكن بعضها مهم. يعطل الوارفارين مثلاً بتحول مجموعة كيتون إلى هدروكسيل بواسطة CYP2A6.
تفاعلات الطور الثاني
- تقاعلات الطور الثاني هي تخليقية (ابتنائية) وتتضمن اقتران (أي إرفاق مجموعة متبادلة)، مما يؤدي عادة إلى مركبات معطلة، رغم أن هناك استثناءات (مثل مستقلب السلفات الفعال للمينوكسيديل، مفعل لقناة البوتاسيوم استعمل لعلاج ارتفاع الضغط الشديد، مورفين-6-غلوكورونيد وهو مستقلب فعال للمورفين طور كعامل مسكن – على الإعطاء الحاد يحرض غثيان وإقياء بشكل أقل من الدواء الأصلي ربما لأنه أكثر قطبية فيفشل في الوصول إلى مراكز الإقياء).
- تحصل تفاعلات الطور الثاني أيضاً في الكبد بشكل أساسي. إذا امتلكت جزيئة الدواء "ممسكاً" ملائماً (مثلاً مجموعة هدروكسيل أو ثيول أو أمينو) سواء كانت في الجزيئة الأصل أو في منتج ناجم عن استقلاب الطور الأول، فإنها عرضة للاقتران.
- المجموعات الأكثر تضمناً هي الغلوكورونيل والسلفات والميثيل والأسيتيل. يمكن أن يقرن الغلوتاثيون ثلثاي الببتيد الأدوية أو مستقلاباتهم من الطور الأول عبر مجموعته السلفهيدريل، كما في إزالة سمية الباراسيتامول.
- يتضمن تشكل الغلوكورونيد تشكل مركب فوسفات عالي الطاقة، يوريدين حمض الغلوكورونيك ثنائي الفوسفات (UDPGA)، والذي ينقل منه حمض الغلوكورونيك إلى ذرة غنية بالالكترونات (N أو S أو O) على الركازة، مشكلاً رابطة أميدية أو إسترية أو ثيول. UDP-glucuronyl transferase الذي يحفز هذه التفاعلات ذو نوعية للركازة واسعة جداً وتضم العديد من الأدوية والجزيئات الغريبة الأخرى.
- كذلك تقترن عدة مواد داخلية المنشأ هامة بنفس الجملة وتضم البيليروبين والستيروئيدات القشرية الكظرية.
- تحصل تفاعلات الأستلة والمثيلة مع acetyl-CoA و S-adenosyl methionine على الترتيب، حيث تعمل على أنها المركبات المعطية. تحصل العديد من تفاعلات الاقتران هذه في الكبد لكن يمكن أن تتضمن أنسجة أخرى مثل الرئة والكلية.
الانتقائية الفراغية
لا ريب أنها فكرة جيدة مع أنه يشكك في فائدة الجهد الموجه نحو تطوير مواد "جديدة" تكون فعلياً فقط المصاوغ الفراغي الفعال من راسيمات مرسخ وآمن. العديد من الأدوية المهمة سريرياً، مثل سوتالول والوارفارين وال[[سيكلوفوسفاميد]، عبارة عن مزائج من المصاوغات الفراغية، والتي لا تختلف مكوناتها في تأثيراتها الفارماكولوجية فقط بل في استقلابها أيضاً، والذي قد يسلك مسالك مختلفة تماماً. تتضمن عدة تداخلات دوائية مهمة سريرياً تثبيط نوعي فراغي لاستقلاب دواء بواسطة دواء آخر. في بعض الحالات، قد تربط سمية الدواء بشكل أساسي إلى أحد مصاوغاته الفراغية وليس بالضرورة المصاوغ الفعال فارماكولوجياً. في الممارسة، حثت السلطات التنظيمية بأن الأدوية الجديدة يجب أن تتألف من مصاوغات فراغية مفردة لتجنب هذه المضاعفات.
تثبيط P450
- تختلف مثبطات P450 في انتقائيتها تجاه أشكال إسوية مختلفة من الأنزيم، وتم تصنيفها حسب آليات تأثيرها.
- تتنافس بعض الأدوية على الموقع الفعال لكنها ليست ركازات (مثلاً الكوينيدين مثبط تنافسي قوي لـ CYP2D6 لكنه ليس ركازة له).
- تضم المثبطات غير التنافسية أدوية مثل الكيتوكينازول الذي يشكل معقداً محكماً مع الشكل Fe+3 لحديد الهيم في CYP3A4، مسبباً تثبيط غير تنافسي عكوس. المثبطات التي تدعى المثبطات المرتكزة على الآلية تتطلب أكسدة بواسطة أنزيم P450. تضم الأمثلة مانع الحمل الفموي gestodene (CYP3A4) والدواء المضاد للديدان diethylcarbamazine (CYP2E1). يرتبط منتج الأكسدة بشكل تساهمي بالأنزيم (مثلاً، الإيبوكسيد المفترض الوسيط للـ gestodene)، فيميل الأنزيم إلى تدمير نفسه (تثبيط انتحاري).
- العديد من التداخلات المهمة سريرياً عبارة عن نتيجة لتثبيط أنزيمات P450.
تحريض الأنزيمات الصغروية
- يزيد عدد من الأدوية، مثل الريفامبيسين والإيثانول والكاربامازبين، فعالية الأكسيداز الصغروي وجمل الاقتران عند إعطائهم بشكل متكرر.
- تمتلك العديد من المواد الكيمائية المسرطنة هذا التأثير أيضاً (مثل benzpyrene, 3-MC)، ويمكن لذلك أن يكون مهماً.
- يمكن أن يزيد التحريض الأنزيمي السمية الدوائية والتسرطن لأن العديد من مستقلبات الطور الأول سامة أو مسرطنة: الباراسيتامول مثال مهم لدواء ذو مستقلب عالي السامية.
استقلاب العبور الأول (الاستقلاب قبل الجهازي)
تُستخلص بعض الأدوية بشكل فعال جداً من الكبد أو جدران الأمعاء بحيث تكون الكمية الواصلة إلى الدوران الجهازي أقل بشكل معتبر من الكمية الممتصة. يعرف هذا باستقلاب العبور الأول أو الاستقلاب قبل الجهازي وهو ينقص التوافر الحيوي حتى عندما يمتص الدواء جيداً. الاستقلاب قبل الجهازي مهم للعديد من الأدوية العلاجية (يظهر الجدول 9.2 بعض الأمثلة)، وهو مشكلة لأن:
- جرعة أكبر بكثير من الدواء مطلوبة عندما يعطى فموياً مقارنة بإعطائه خلالياً
- يوجد اختلافات فردية ملحوظة في مدى استقلاب العبور الأول.
المستقلبات الدوائية الفعالة فارماكولوجياً
الجدول 9-2. أمثلة لأدوية تخضع لإزالة عبور أول كبيرة
| Aspirin |
|---|
| Metoprolol |
| Glyceryl trinitrate |
| Isosorbide dinitrate |
| Levodopa |
| Morphine |
| Propranolol |
| Levodopa |
| Salbutamol |
| Verapamil |
| Lidocaine |
الجدول 9-3 بعض الأدوية التي تنتج مستقلبات فعالة أو سامة
| Inactive (prodrugs) | Active drug | Active metabolite | Toxic metabolite |
|---|---|---|---|
| Azathioprine → | Mercaptopurine | ||
| Cortisone → | Hydrocortisone | ||
| Prednisone → | Prednisolone | ||
| Enalapril → | Enalaprilat | ||
| Zidovudine → | Zidovudine trisphosphate | ||
| Cyclophosphamide → | Phosophoramide mustard → | Acrolein | |
| Diazepam → | Nordiazepam → Oxazepam | ||
| Morphine → | Morphine 6-glucuronide | ||
| Halothane → | Trifluoroacetic acid | ||
| Methoxyflurane → | Fluoride | ||
| Paracetamol → | N-Acetyl-p-benzoquinone imine |
- لا يصبح الدواء فعال فارماكولوجياً أحياناً إلا بعد خضوعه للاستقلاب (انظر الجدول 9.3). مثلاً الآزاثيوبرين، دواء كابت للمناعة، يستقلب إلى ميركابتوبورين، وإينالابريل مثبط للأنزيم المحول للأنجيوتنسين يحلمه إلى شكله الفعال إينالابريلات.
- تدعى هذه الأدوية التي يكون فيها الدواء الأصلي لها فاقداً الفعالية، بطلائع الأدوية prodrugs.
- تصمم هذه الأدوية أحياناً بشكل مقصود للتغلب على مشاكل إيصال الدواء.
- يمكن أن يغير الاستقلاب التأثيرات الفارماكولوجية لدواء بشكل كيفي. يثبط الأسبرين بعض وظائف الصفيحات ويمتلك فعالية مضادة للالتهاب. يحلمه إلى حمض الصفصاف، الذي يمتلك فعالية مضادة للالتهاب لكن لا يمتلك فعالية مضادة للصفيحات.
- في أمثلة أخرى، تمتلك المتسقلبات تأثيرات فارماكولوجية مشابهة لتأثيرات المركب الأصلي (مثل البنزوديازبينات، حيث يشكل العديد منها مستقلبات فعالة مديدة العمر يمكن أن تؤدي إلى تركين يستمر بعد زوال الدواء الأصلي).
- هناك أيضاً حالات تكون فيها المستقلبات مسؤولة عن السمية. السمية الكبدية للباراسيتامول مثال عنها، والسمية المثانية للسيكلوفوسفاميد، الناجمة عن مستقلبه السام آكرولئين، مثال آخر. يظهر الميثانول والإيثلين غليكول تأثيراتها السامة عبر مستقلباتها المتشكلة بواسطة نازعة هدروجين الكحول. يعالج التسمم بهذه العوامل بالإيثانول (أو مثبط أكثر قوة) حيث يتنافس على الموقع الفعال من الأنزيم.
- يثبط ديسيلفيرام Disulfiram CYP2E1 وينقص بالتالي تشكل ثلاثي فلورو حمض الخل أثناء التخدير باستعمال الهالوثان، فيرفع من فرصة منع التهاب الكبد بالهالوثان.
الإطراح
الطريق الأكثر شيوعاً للإطراح: هو عبر الكليتان، وقد يتم الإطراح أيضاً عبر الرئتين وحليب الإرضاع والجهاز الهضمي والصفراء و اللعاب.
الإفراغ الصفراوي والدوران الكبدي المعوي
- تنقل الخلايا الكبدية مختلف المواد، بما فيها الأدوية، من البلازما إلى الصفراء بواسطة جمل ناقلة مشابهة لجمل النبيب الكلوي وتضم ناقلات الكاتيونات العضوية (OCTs)، ناقلات الأنيونات العضولية (OATs) و P-glycoproteins (P-gp).
- تركز مختلف الاقترانات الدوائية المحبة للماء (خاصة الغلوكورونيدات) في الصفراء وتوصل إلى الأمعاء، حيث يتحلمه الغلوكورونيد عادة محرراً الدواء الفعال، ومرة أخرى يمكن أن يعاد امتصاص الدواء الحر وتكرر الحلقة (الدوران الكبدي المعوي).
- يولد هذا التأثير "مخزون" من الدواء معاد الدوران ويمكن أن تكون كميته حتى 20% من الدواء الكلي في الجسد ويطيل التأثير الدوائي.
- تشمل الأمثلة التي يكون فيها مهماً المورفين والإيثينل استراديول. تفرز عدة أدوية بمجال كبير في الصفراء.
- Vecuronium (مرخي عضلي غير نازع للاستقطاب) مثال عن دواء يفرع بشكل رئيسي غير متغيراً في الصفراء. يمتص الريفامبيسين من الأمعاء ويزال الأستيل ببطء، محتفظاً بفعاليته البيولوجية.
- يفرز الشكلين في الصفراء، لكن الشكل مزال الأسيتيل لا يعاد امتصاصه لذا يغادر معظم الدواء الجسم في النهاية بهذا الشكل في البراز.
الإفراع الكلوي للدواء والمستقلبات
تختلف الأدوية بشكل كبير في المعدل الذي تفرغ به عبر الكلية، إذ يتراوح من البنسلين الذي يصفى من الدم بشكل كامل تقريباً بنقلة كاملة عبر الكلية إلى الديازيبام، الذي يصفى ببطء شديد جداً. تقع معظم الأدوية بين هاتين النهايتين، وتصفى المستقلبات دائماً (تقريباً) بشكل أسرع من الدواء الأصل. يوجد 3 عمليات أساسية تحتسب للإفراغ الدوائي الكلوي:
- الرشح الكبيبي
- الإفراز النبيبي الفعال
- الانتشار المنفعل عبر الظهارة النبيبية
الرشح الكبيبي
- تسمح الشعيرات الكبيبية للجزيئات الدوائية ذات الوزن الجزيئي تحت الـ 20 000 بالعبور إلى الرشاحة الكبيبية.
ألبومين البلازما (ذو وزن جزيئي تقريباً 68000) غير نفوذ تماماً تقريباً، لكن تعبر معظم الأدوية، باستثناء الجزيئات الكبروية مثل الهيبارين والمركبات البيولوجية، الحاجز بشكل حر إذا ارتبط دواء بألبومين البلازما، يرشح الدواء الحر فقط. إذا كان دواء، مثل الوارفارين، مرتبطاً بنسبة 98% إلى الألبومين، سيكون تركيزه في الرشاحة فقط 2% من تركيزه في البلازما، وتنخفض كذلك التصفية بالترشيح.
الإفراز النبيبي
- لأن الرشاحة تتضمن حركة إسوية الضغط التناضحي لكل من الماء والذوائب، لا يؤثر ذلك على التركيز الحر للدواء في البلازما.
- بالتالي لا يختل التوازن بين الدواء الحر والمرتبط، ولا يوجد ميل لانفكاك الدواء المرتبط عندما يعبر الدم الشعيرات الكبيبية. بالتالي ينخفض معدل تصفية دواء مباشرة بالتناسب مع الجزء المرتبط.
- في حالة الإفراز النبيبي الفعال، لا تكون هذه الحالة؛ فقد يتأخر الإفراز قليلاً حتى لو كان الدواء مرتبطاً. ذلك لأن الحوامل تنقل جزيئات الدواء غير مصحوبة بالماء. بقبط جزيئات الدواء الحرة وبالتالي ينخفض تركيز البلازما الحر مؤدياً إلى انفصال الدواء المرتبط من ألبومين البلازما. النتيجة هي أن 100% من الدواء، حراً أو مرتبط، متوفر للحامل.
- يرشح حتى 20% من التدفق البلازمي الكلوي عبر الكبيبات، تاركاً على الأقل 80% من الدواء الموصل ليعبر الشعيرات المحيطة بالنبيبات للنبيب القريب. هنا تنقل جزيئات الدواء إلى اللمعة النبيبية بواسطة جملتين حاملتين مستقلتين ونسبياً غير نوعيتين. إحداها هي الـ OAT تنقل الأدوية الحمضية (بالإضافة إلى مختلف الحموض داخلية المنشأ مثل حمض البول) والأخرى OCT تتعامل مع الأسس العضوية. بعض الأدوية المهمة التي تنقل بهاتين الجملتين موجودة في الجدل 9.4.
- يمكن لحامل الـ OAT أن ينقل الجزيئات الدوائية عكس مدروجها الكهربائي الكيميائي ويمكنه بالتالي تخفيض التركيز البلازمي إلى الصفر، في حين تسهل OCT النقل مع المدروج الكهربائي الكيميائي. لأن 80% من الدواء المنقول إلى الكلية يتواجد على حامل، فإن الإفراز النبيبي الآلية الأكثر فعالية لإطراح الدواء كلوياً. بعكس الرشح الكبيبي، يمكن أن يحقق النقل المتواسط بحامل تصفية دوائية عظمى حتى لو كان معظم الدواء مرتبطاً ببروتين بلازمي.
- البنسلين مثلاً، رغم أن 80% منه مرتبط بالبروتين، وبالتالي لا يمكن تصفيته بالترشيح إلا ببطء، إلا أنه يزال بشكل كامل تقريباً بالإفراز النبيبي القريب وبالتالي فإطراحه سريع.
تتنافس العديد من الأدوية على نفس الجملة الناقلة (الجدول 9.4)، مؤدية إلى تداخلات دوائية. مثلاً طور بروبينيسيد أصلأً لإطالة تأثير البنسلين بتأخير إفرازه النبيبي.
الانتشار عبر النبيب الكلوي
- يعاد امتصاص الماء بعبور السائل النبيب، حجم البول الخارج فقط حوالي 1% من حجم الرشاحة الكبيبية. بالتالي إذا كان النبيب نفوذاً بشكل حر لجزيئات الدواء فإن حوالي 99% من الدواء المرتشح سيعاد امتصاصه بشكل منفهل نتيجة مدروج التركيز.
- لهذا فإن الأدوية المنحلة بالدسم تفرغ بشكل ضعيف في حين أن الأدوية القطبية ذات النفاذية النبيبية المنخفضة تبقى في اللمعة وتصبح مركزة أكثر فأكثر بإعادة امتصاص الماء.
- تضم الأدوية التي تعامل بهذه الطريقة الديجوكسين والصادات الحيوية الأمينوغليكوزيدية. هذه أمثلة عن مجموعة صغيرة نسبياً من الأدوية لكنها مهمة (الجدول 9.5) والتي لا تعطل بالاستقلاب، إنما معدل الطرح الكلوي هو العامل الأساسي الذي يحدد مدة تأثيرها. تستعمل هذه الأدوية بحرص لدى الأفراد الذين تكون وظيفتهم الكلوية قاصرة، ويشملون المسنين والمرضى الذين يعانون من مرض كلوي أو أي مرض حاد شديد.
الجدول 9-4 أدوية مهمة ومواد مرتبطة تفرز إلى النبيب القريب الكلوي بواسطة نواقل OAT أو OCT
| OAT | OCT |
|---|---|
| p-Aminohippuric acid | Amiloride |
| Furosemide | Dopamine |
| Glucuronic acid conjugates | Histamine |
| Glycine conjugates | Mepacrine |
| Indometacin | Morphine |
| Methotrexate | Pethidine |
| Penicillin - Probenecid | Quaternary ammonium compounds |
| Sulfate conjugates | Quinine |
| Thiazide diuretics | 5-Hydroxytryptamine (serotonin) |
| Uric acid | Triamterene |
الجدول 9-5 أمثلة عن أدوية تفرز بشكل كبير غير متغيرة في البول
| Percentage | Drugs excreted |
|---|---|
| 100-75 | Furosemide, gentamicin, methotrexate, atenolol, digoxin |
| 75-50 | Benzylpenicillin, cimetidine, oxytetracycline, neostigmine |
| ∼50 | Propantheline, tubocurarine |
درجة تأين العديد من الأدوية الحمضية الضعيفة أو الأساسية الضعيفة معتمدة على الـ pH ويؤثر ذلك بشكل ملحوظ على إفراغهم الكلوي. يعني التأثير الحاصر الأيوني أن دواءً أساسياً يفرغ بشكل أكثر سرعة في بول حمضي الذي يتحيز للشكل المشحون وبالتالي يثبط إعادة الامتصاص. بالعكس، تفرغ الأدوية الحمضية بشكل أكثر سرعة إذا كان البول قلوياً. تستعمل قلونة البول لتسريع إفراغ الصفصفات في معالجة حالات خاصة من فرط جرعة الأسبرين.
التصفية الكلوية
〖CL〗r=(Cu×Vu)/Cr
أفضل طريقة لقياس كمية إطراح الأدوية بالكليتين هي التصفية الكلوية CLr. وتعرف بأنها حجم البلازما الحاوية على كمية المادة المزالة من الجسم بواسطة الكليتين في وحدة الزمن. تحسب من تركيز البلازما Cp والتركيز البولي Cu ومعدل تدفق البول Vu وبالمعادلة: تتغير CLr بشكل كبير لأدوية مختلفة من أقل من 1 مل/الدقيقة إلى الحد النظري الأقصى بالتدفق البلازمي الكلوي والذي يقارب 700 مل/الدقيقة مقاساً بتصفية حمض p-aminohippuric (PAH) (يصل الاستخلاص الكلوي لـ PAH 100%).
أنظر أيضا
- علم تأثير الأدوية
- ديناميكية دوائية
- عمر النصف الحيوي
- توافر بيولوجي
- حيز (حركية دوائية)
- نظام تصنيف الصيدلانيات البيولوجية
وصلات خارجية
- برامج الحركيات الدوائية
- برنامج بايوكنيكا
- معلومات عامة عن الحركيات الدوائية
- معلومات إضافية عن الحركيات الدوائية