أميد
اذهب إلى التنقل
اذهب إلى البحث
الأميدات
تحضير الأميدات
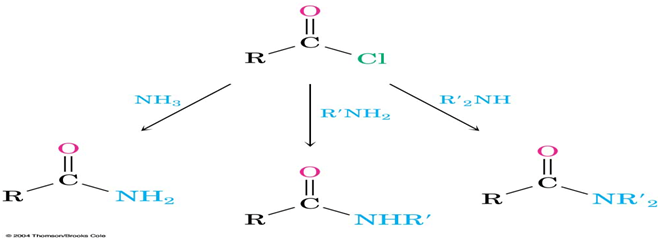
بما أن كلوريدات الحموض هي الأكثر فعالية تجاه تفاعلات النكليوفيل فابتداء منها نستطيع تحضير الكثير من المركبات وأحدها الأميدات.
- نلاحظ الأميدات الناتجة مركبات صلبة سهلة التشخيص (بالبلورة أو قياس درجة الانصهار)
- نلاحظ أننا لم نستخدم الأمين الثالثي لأننا نريد H.
تفاعلات الأميدات
- تفاعلات الأميدات محدودة :
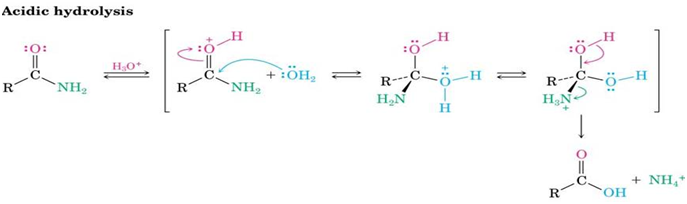
- حلمهة الأميدات:
- تحتاج شروط قوية لأنها أكثر ثباتاً وتتم بوساطة حمضية أو قلوية كما يلي:
- في الحلمهة الحمضية: يتشكل حمض و أمونيوم NH4+
- أما في الحلمهة القلوية: يتشكل ملح وأمونيا (نشادر)
عند حلمهة البروتينات (بولي ببتيد) : تعطي حموض أمينية + نشادر
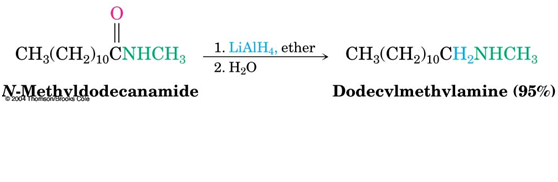
- إرجاع الأميدات: (إرجاع الأميدات إلى أمينات)
NH2 ليست سهلة الرحيل , لذلك نستخدم مرجع قوي هو LiALH4 ثم نضيف الماء فنحصل على أمين بحسب الأميد
نجري التفاعل في وسط لا مائي ( المرحلة الأولى ) لتلافي الانفجار.
لاحظ استخدمنا أميد ثانوي فسوف نحصل على أمين ثانوي
ملاحظات:
- الأميدات هي الأكثر مقاومة : أميدات > استرات > بلاماء الحموض > كلوريدات الحموض
- لهذا التفاعل أهمية خاصة فلو كان لدينا مشتق دوائي على شكل استر فسوف يتفكك مباشرة في الجسم لأن الوظيفة الاسترية فعالة أما إذا حولناه إلى أميد فهذا يزيد من مقاومة الدواء و إعطاء تأثيرات طويلة الأمد وجهازي.
RCOOR→ RCH_2 OH+R’OH
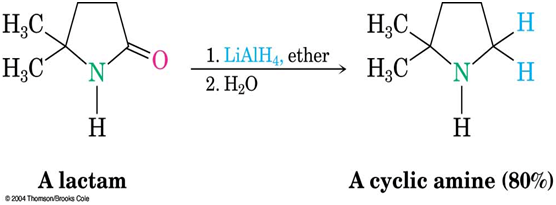
- إرجاع الأميد الحلقي:
يدعى الأميد الحلقي بLactam (يشتق من البيرول), يعطي اللاكتام بإرجاعه أمين حلقي.