الفرق بين المراجعتين لصفحة: «رقعة تغذية»
ط (مراجعة واحدة) |
(لا فرق)
|
المراجعة الحالية بتاريخ 16:05، 5 نوفمبر 2013

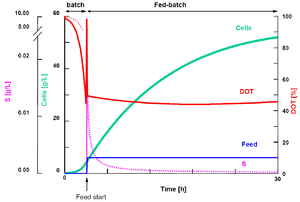
تمثل رقعة أو دفعة التغذية عملية دفعةٍ تقانية حيوية والتي تُعَدُ قائمةً على مبدأ تغذية ركيزة مغذية محددة للنمو إلى المزرعة البكتيرية. حيث تستخدم استراتيجية رقعة التغذية عادةً في العمليات الصناعية الحيوية للوصول إلى كثافةٍ عاليةٍ للخلية في المفاعل الحيوي. ونلاحظ أن غالبية المحاليل المغذية تُعَدُ عالية التركيز لتجنب ترقيق أو تخفيف المفاعل الحيوي. كما تؤثر الإضافة المسيطر عليها باستمرار للممغذيات على معدل نمو المزرعة البكتيرية وتسمح بتجنب التدفق الزائد للآيض (بالإنجليزية: Crabtree effect) (المتمثل في تكوين الآيضات الجانبية والتي منها الخلات لل إشريكية القولونية، حمض اللاكتيك في مزارع الخلية، والإيثانول في خميرة فطريات السكر (بالإنجليزية: Saccharomyces cerevisiae))، وكذلك لتجنب الحد من الأكسجين (انظر كائن لاهوائي).
وهنا يوفر تحجيم الركيزة القدرة على ضبط معدلات التفاعل لتجنب القيود التقنية المتصلة بتبريد المفاعل ونقل الأكسجين. هذا ويسمح تحجيم الركيزة بالسيطرة الآيضية، لتجنب تأثيرات التناضح، القمع المقيض (بالإنجليزية: catabolite repression) وكذلك تدفق تيار الآيض للمنتجات الثانوية.
استخدام العديد من الاستراتيجيات المختلفة للتحكم في النمو داخل عملية رقعة (دفعة) التغذية:
| معامل السيطرة | مبدأ السيطرة |
|---|---|
| DOT (pO2) | DOstat (DOT= ثابت), F~DOT |
| معدل استهلاك الأكسجين (OUR) | OUR=ثابت, F~OUR |
| الغلوكوز | مقياس الغلوكوز الإلكتروني (FIA), غلوكوز=ثابت |
| الاسيتات (خلات) | مقياس الأسيتات الإلكتروني (FIA), الأسيتات=ثابت |
| الآس الهيدروجيني (pHstat) | F~pH (ارتباط التحمض بنسبة الغلوكوز المرتفعة) |
| الأمونيا | مقياس الأمونيا الإلكتروني (FIA), الأمونيا=ثابت |
| درجة الحرارة | T المعدلة وفقاً لـ OUR أو pO2 |
المصادر
- Hewitt CJ, Nienow AW: The scale-up of microbial batch and fed-batch fermentation processes. Adv Appl Microbiol 2007, 62:105-135.
- Wlaschin KF, Hu WS: Fedbatch culture and dynamic nutrient feeding. Cell Culture Engineering 2006, 101:43-74.
- Shiloach J, Fass R: Growing E. coli to high cell density--a historical perspective on method development. Biotechnol Adv 2005, 23:345-357.
- Panda AK: Bioprocessing of therapeutic proteins from the inclusion bodies of Escherichia coli. Adv Biochem Eng Biotechnol 2003, 85:43-93.
- Liden G: Understanding the bioreactor. Bioprocess and Biosystems Engineering 2002, 24:273-279.
- Neubauer P, Winter J: Expression and fermentation strategies for recombinant protein production in Escherichia coli. In: Merten OW et al. (Eds). Recombinant Protein Production with prokaryotic and eukaryotic cells. A comparative view on host physiology. 2001, Kluwer Academic Publisher, Dortrecht, The Netherlands. pp. 196-260.
- Balbas P: Understanding the art of producing protein and nonprotein molecules in Escherichia coli. Molecular Biotechnology 2001, 19:251-267.
- Lee J, Lee SY, Park S, Middelberg AP: Control of fed-batch fermentations. Biotechnol Adv 1999, 17:29-48.
- Zhang J, Greasham R: Chemically defined media for commercial fermentations. Applied Microbiology and Biotechnology 1999, 51:407-421.
- Lee SY: High cell-density culture of Escherichia coli. Trends Biotechnol 1996, 14:98-105.
- Mendozavega O, Sabatie J, Brown SW: Industrial-Production of Heterologous Proteins by Fed-Batch Cultures of the Yeast Saccharomyces-Cerevisiae. Fems Microbiology Reviews 1994, 15:369-410.
- Yee L, Blanch HW: Recombinant protein expression in high cell density fed-batch cultures of Escherichia coli. Biotechnology (N Y ) 1992, 10:1550-1556.
- Riesenberg D, Schulz V: High-cell-density cultivation of Escherichia coli. Curr Opin Biotechnol 1991, 2:380-384.